溶瘤病毒肿瘤治疗进展和投资方向初探
文 | 曹锋,华医资本创始合伙人,博士,拥有丰富的医药领域知识和医药品牌的管理营销经验,成功管理10多个品牌营销,现在主要研究方向集中在国内外新兴医疗技术市场转化。基于专业的视野和严密的医疗投资逻辑,投资了众多医疗项目
注:原文发表于《张江评论》
1912 年,一名被狗咬伤的女士向医生求救,要求医生为自己接种狂犬疫苗。在随后的复查中,医生发现原本存在于女子体内的子宫颈瘤大幅缩小了。溶瘤病毒治疗肿瘤的概念在此偶发的事件中被提出。
1949 年,运用血清中提取的肝炎病毒,人们成功地治愈了22例淋巴瘤患者。1950年到 1980年,大量临床试验对一些野生型或减毒溶瘤病毒株(如西尼罗河病毒、肝炎病毒、黄热病毒、腺病毒等)进行了验证,由于当时技术条件的限制,试验结果非常不理想。
但是,人们对溶瘤病毒治疗肿瘤的探索一直没有停止。
市场动态
临床试验和对溶瘤病毒机制的探索发现,溶瘤病毒可能存在3种治疗癌症的机制。
第一,溶瘤病毒直接杀伤肿瘤细胞。
第二,溶瘤病毒改善肿瘤的免疫微环境,激发人体的抗肿瘤免疫。因为溶瘤病毒除了能特异性靶向溶解肿瘤细胞外,还能通过上调炎症因子,释放肿瘤抗原来促进人体抗肿瘤免疫应答,也就是经常说的“冷肿瘤”转变为“热肿瘤”。
第三,溶瘤病毒作为一个基因治疗的平台,使肿瘤细胞内源性表达抗肿瘤药物。
截至 2018 年,两种基因改造治疗性溶瘤病毒株获得上市批准。
2005年,用于治疗黑色素瘤的腺病毒安柯瑞(H101)获中国上市批准。
安进(Amgen)公司的 T-VEC(Talimogene laherparepvec,商品名 Imlygic)首先于 2015年10月获得美国食品药品监督管理局(FDA)的批准,随后分别于2016年1月和 2016年5月获得欧洲和澳大利亚的上市许可。
2018 年,溶瘤病毒领域的几次重大收购再次引发热度。
2018年5月,美国强生公司斥资10亿美元收购生物制药公司BeneVir Biopharm。2018年7月,天津天士力公司斥资4800万美元与法国生物公司 Transgene合作,涉及的T601 和T101两种免疫治疗药物由 ransgene-Tasly 合资公司在中国开发。
T601 是下一代溶瘤免疫疗法,基于T601中集成的转基因专利套件,被设计用于诱导癌细胞的分解(溶瘤作用)并允许在肿瘤中局部产生氟尿嘧啶(5-F U)。2018年9月,勃林格殷格翰公司收购奥地利的溶瘤病毒公司Viral therapeutics。
溶瘤病毒的局限性
值得注意的是,目前溶瘤病毒治疗肿瘤在给药方式、靶向性、溶瘤效力和人体免疫中和等方面存在一定的局限性。已上市的溶瘤病毒T-VEC 销售情况并不乐观。根据安进公司 2017 年的财务报表数据,T-VEC的全球销售额在 5000 万美元左右。
●给药方式
现阶段溶瘤病毒的给药方式大多是以瘤内注射为主,瘤内注射在效果上可以防止病毒在体内运输中遭受人抗体的中和,保证溶瘤病毒安全到达病灶位点。
但是,其缺点也非常明显,一些位置较为隐蔽的肿瘤位点很难进行肿瘤内给药,如脑癌。而且,瘤内注射在临床操作上也不够便捷,普通护士无法进行瘤内注射操作,推广遇到的障碍较多。
●靶向性
每种病毒在增强靶向性上都有自己的方式,如腺病毒 E1B 位点的敲除。但是,对于一些病毒的系统给药试验中,靶向性不强导致的不良反应依然十分常见,如使用 T-VEC后的皮疹。因此,增强靶向性是系统给药的必要条件。
●溶瘤效力和人体免疫中和
现阶段的溶瘤病毒大多数是减毒病毒框架,如已上市的T-VEC敲除了复制调控基因 ICP27,这使得病毒的复制效率和溶瘤效率下降。
在减毒病毒溶瘤释放之后,机体自身免疫系统会比较容易地清除这些减毒病毒,从而无法达到相应的溶瘤效果。
另外,广泛使用的免疫调控因子粒细胞巨噬细胞集落因子(GM-CSF)临床效果不佳。因此,如何解决人体的抗病毒免疫而激发抗肿瘤免疫是现阶段溶瘤病毒最大的难题。
未来趋势分析
溶瘤病毒在未来发展的趋势有几个主要方向:更加便捷、有效的给药方式的开发;溶瘤病毒联合其他肿瘤疗法的开发;基因工程病毒,通过基因编辑为病毒“武装”多个细胞毒性或免疫调控基因。
●给药方式
在给药方式上,由于静脉注射操作简便,能更容易到达隐蔽的肿瘤位点,将是溶瘤病毒应用的主流方向。
但是,系统给药对溶瘤病毒本身的要求也更高,因此对溶瘤病毒静脉注射的研究探索也很多。例如,加拿大公司 Oncolytics Biotech的病毒性疗法Reolysin利用的呼肠孤病毒在静脉注射之后,会利用血细胞躲避血清中的抗体中和作用。
另外,可以利用纳米材料、病毒衣壳改造等方式对病毒进行改造来躲避给药时遇到的免疫系统攻击,比如修饰腺病毒的衣壳蛋白降低其抗原性。
●基因工程病毒
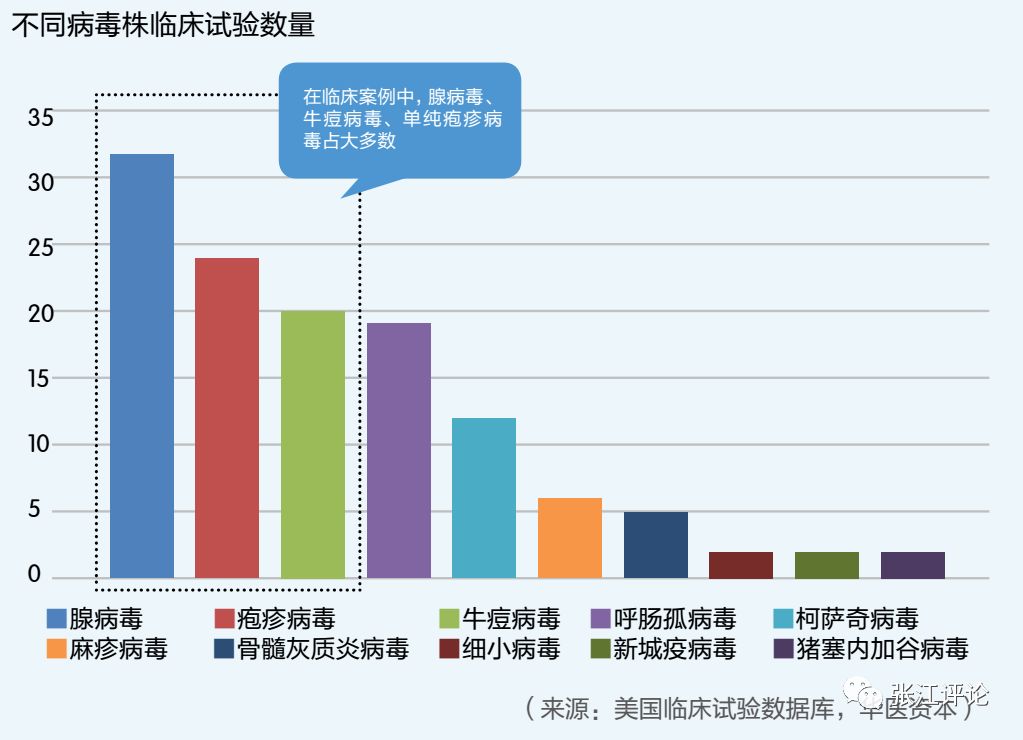
FDA临床审批的数据显示,目前124例公开的临床试验中,腺病毒 32例,疱疹病毒 24例,牛痘病毒20例,呼肠孤病毒19例,柯萨奇病毒12例,其他病毒17 例。
其他病毒包括骨髓灰质炎病毒5例,新城疫病毒2例,麻疹病毒6例,细小病毒2例,猪塞内加谷病毒 2 例。其中,可进行基因工程病毒株的研究达到 35 例,占据很大一部分。
在临床案例中,腺病毒、牛痘病毒、单纯疱疹病毒占大多数。究其原因,首先是这三种病毒能进行大片段的基因改造,有更加广阔的提升空间;其次是基因工程病毒经常作为基因载体,研究得较为透彻,更加容易控制效果。
野生型病毒改造无法如此直接,而基因工程病毒能通过不同的位点修饰分别提高自身效力、靶向性及促发免疫系统的能力。
●免疫因子编辑
除了溶瘤效力之外,影响溶瘤病毒疗效的因素在于人体的抗病毒免疫限制。加入免疫调控因子是为了将人体的抗病毒免疫转化成抗肿瘤免疫。
临床研发最久并在大范围应用中加入了溶瘤病毒的粒细胞巨噬细胞集落因子(GM-CSF),已被临床证明效果有限。正在研发的携带免疫调控因子的溶瘤病毒,如腺病毒携带 IL12、IL-15、IL24,疱疹病毒携带 IFN-β、IFN-γ,这些细胞因子在免疫调控机制中发挥着招募免疫细胞的功能,更有溶瘤病毒携带 PD-1/PD-L1 抑制蛋白基因来改善肿瘤免疫微环境。这些方案是学界探索的方向之一,但需要进一步临床试验的验证。
●联合疗法
综合目前各个癌症领域的临床表现来看,溶瘤病毒治疗存在“新一代溶瘤病毒尚未进入 II 期和 III期临床,老一代溶瘤病毒单药效果不佳”的现象。
因此,众多医药巨头尝试开发协同免疫疗法或联合化疗的联合方案。
究其原因,一是联合用药方案已经成为癌症治疗中的一个趋势;
二是溶瘤病毒本身能够促进肿瘤免疫环境的改善,弥补了现阶段肿瘤免疫疗法的局限性,希望能产生“1+1>2”的效果。从目前来看,在溶瘤病毒领域有较大突破的往往是联合疗法。
相关主要肿瘤研究进展
●肺癌
目前在临床阶段针对肺癌的溶瘤病毒共有10例。
单药方面,肺癌3例单药开始时间都在2012年之前,均未有结果披露。Reolysin 已完成 II 期单药临床,未发现有后续的单药 III 期临床在进行,预测结果不理想。
联合疗法中唯一有结果的是Reolysin 联合紫杉醇化疗治疗的I期临床,结果显示,Reolysin 的加入并没有对疗效有很大的提升。
2012年开始的 Reolysin 联合化疗对经过治疗的晚期非小细胞肺癌 II 期临床试验也已经完成,结果未披露。总体看来,没有表现突出的临床试验。
在较早期的试验中,可以期待Maraba病毒和VSV-IFNβ-NIS疱疹病毒。Maraba 病毒在基因组中加入了肿瘤抗原的基因,而VSV-IFNβ-NIS则加入了 IFNβ 免疫调控基因。
它们在如何将人体的抗病毒免疫转化成人体的抗肿瘤免疫这一问题上有不同的创新,但需要进一步临床结果的验证。
重点关注案例:Maraba 病毒和VSV-IFNβ-NIS 疱疹病毒 I 期临床。
●肝癌
肝癌是中国患病新增人数第二高的癌症,并且 5 年生存率非常低。临床阶段的溶瘤病毒案例有8例。
单药方面,JX594在2013 年的临床结果未能达到总体生存期的主要终点,被评为低于平均。随后JX594 的研发主要以联合疗法为主。
在联合疗法中,可重点关注正在进行的 JX-594 联合索拉菲尼化疗的 III 期临床。虽然 II 期临床试验结果未公布,但是能够进入 III 期临床,可以预测 II 期临床结果不错,III 期临床结果值得期待。
处于较早期的 JX-594 联合 PD-1的 I/II 期临床试验,CVA21 联合免疫疗法 I 期临床试验,以及 VSV 病毒联合免疫疗法都是在 2018 年开始的,未有结果披露。
重点关注案例:JX-594 联合索拉菲尼化疗(III 期临床招募中)。
●胰腺癌
胰腺癌发病人数比不上肝癌和肺癌,5年生存率总体在10%左右,但因为难治愈、致死率高,也被称为“癌症之王”。
近年来,免疫疗法的兴起似乎让人们看到了攻克癌症的希望。但是,许多临床结果证明,免疫疗法在胰腺癌上依然没有实质性的突破,这与胰腺癌组织本身特殊性有关。
胰腺癌微环境常表现为免疫抑制细胞增多、免疫细胞失活以及低肿瘤突变负荷(TMB)。目前,在研溶瘤病毒临床数量为9例。
单药方面,3个临床试验都处在I期,属于早期临床。HF10是带有GM-CSF扩增子和GM-CSF细胞因子的病毒,对比T-VEC能更加有效、大量地表达GM-CFS。
2018 年 , 其 I期临床结果披露,显示出一定疗效,但对比现有疗法疗效突破不大,可以关注其后续的临床进展。其他两个单药试验是装备了IL12的腺病毒和一款靶向性进行过基因改造的牛痘病毒,这两个临床试验都处于招募状态。
联合疗法方面,Reolysin 联合化疗的结果显示,Reolysin 的加入未能提高最终治疗效果。Reolysin尝试联合 Pembrolizumab 疗法,现在处于 II 期临床招募阶段,可以关注其临床进展。
重点关注案例:HF10 单药 I 期临床,Reolysin 联合 Pembrolizumab二线治疗 (II 期临床招募中 )。
●黑色素瘤
黑色素瘤属于皮肤癌的一种,黑色素瘤的 5 年生存率相对较高。目前,溶瘤病毒用于黑色素瘤的临床研究较多。
单药方面,T-VEC的单药试验显示其总缓解率在23.3%,疗效对比目前的一线疗法 Keytruda 免疫疗法有一定差距。
CVA21 的 II 期单药试验也已经完成,结果较为一般,在黑色素瘤单药方面 CVA21 无后续进展。联合疗法方面有一定的突破,CVA21 联合 Ipilimumab 总缓解率在72%,T-VEC 联 合 Pembrolizumab I期临床的 21 人中,总缓解率达到62%,完全缓解率达到 33%。
相比一线疗法 Pembrolizumab 单药缓解率30% ~ 40%有明显提高。在其余的临床案例 中,Reolysin 联合化疗的 II 期试验结果显示,Reolysin的加入并没有明显改善化疗的疗效。
其余联合疗法均是近几年进行的,HF10、ONCOS-102依然装备的是较落后的GM-CSF,单药希望不大,可以关注其联合免疫疗法临床结果。
重点关注案例:CVA21联合Ipilimumab的I期临床,T-VEC联合 Pembrolizumab的III期临床。
●乳腺癌
乳腺癌是常见的女性肿瘤之一。在发达国家乳腺癌 5 年治愈率为80%~90%,在发展中国家生存率稍差。
单药方面,临床阶段的溶瘤病毒案例共有3例。Reolysin单药治疗晚期乳腺癌的 II 期临床已完成,但结果未披露。HF10完成 I 期临床后没有在乳腺癌上进行后续的临床试验。
联合用药方面,临床结果最有前景的是 Reolysin 联合紫杉醇/卡铂化疗,II 期临床结果在总体生存期上比标准化疗有显著提升。该疗法也因此得到 FDA 快速通道的审批。
在近几年才开始进行的临床案例中,CAdVEC 联合CAR-T 的I期临床试验正在进行,该联合疗法也是一个全新的尝试方向。CAdVEC 基因组中加入了PD-L1的抑制多肽基因,这一策略试图解决CAR-T疗法中T细胞无法浸润杀伤实体瘤的困局,我们非常期待其临床表现。
重点关注案例:Reolysin与紫杉醇联用疗法(II 期临床完成),CAdVEC 联合CAR-T的 I 期临床。
●膀胱癌
单药方面,CG0070是一款加入了GM-CSF的腺病毒,临床已进入III 期,但试验已经终止,其余的CG0070 临床试验或取消或终止,预测单药效果不佳。
联合疗法方面,除了文中提到的CAdVEC联合CAR-T之 外,Reolysin 联合吉西他滨化疗I 期临床试验取消,预计结果不佳。ColoAd和 Enadenotucirev 两款腺病毒,还处于机理验证和剂量试验阶段,属于非常早期的探索阶段。
重点关注案例:CAdVEC 联合CAR-T的 I 期临床。
前景可期
评价一款溶瘤病毒应该以其临床表现对比该适应证一线/二线标准疗法为基础评判准则,辅助其本身在给药方式、靶向性、溶瘤效力、改善免疫环境(如避免人体免疫攻击)等自身特性上的创新进行评估。
总体来看,老一代溶瘤病毒自身还存在着一些问题,如给药方式繁琐、减毒病毒溶瘤效果差、人体免疫中和限制其效果、GM-CSF临床效力有限等。
因此,老一代溶瘤病毒单药临床表现一般,几乎所有有突破的溶瘤病毒案例均是联合疗法方案。
而新一代溶瘤病毒正在研发中,大部分还处于临床早期,相比已上市的 T-VEC 和研发较多的 JX-594、Reolysin,新一代溶瘤病毒除了在溶瘤效力和靶向性上的改进之外,更加注重有效的免疫调控因子的加入,更有溶瘤病毒加入了多重免疫因子,研发界也认为这是值得探索的方向之一,期待未来的临床结果的验证。
从投资的角度来看,老一代溶瘤病毒单药效力不稳定,业界更加关注溶瘤病毒在改善肿瘤免疫微环境上的作用,开发方向主要以联合疗法为主。但是,新一代溶瘤病毒还处于临床试错阶段,临床结果不稳定,可持续关注临床试验的进展。